
近日,我所仿生催化合成研究组(211组)陈庆安研究员团队在非天然手性环状单萜构建研究方面取得新进展。该团队基于仿生催化理念,通过廉价Ni金属催化剂,利用大位阻手性氮杂环卡宾配体,高效合成了一系列非天然手性环状单萜及其衍生物。
萜类化合物是一类广泛存在于生物体内并具有异戊二烯单元的天然产物,由于其具有重要的生理活性,萜类化合物的合成与转化是生物体内最重要的代谢途径之一。在生物合成中,这些成千上万的萜类化合物大部分均衍生于两个C5合成砌块:异戊烯基焦磷酸(IPP)和二甲烯丙基焦磷酸(DMAPP)。这两个C5单元可以相互耦合成焦磷酸香叶酯(GPP),然后在酶催化下通过环化、重排或偶联等反应,生成多样性的开链或环状萜类化合物。单萜及其衍生物作为其中最具代表性萜类化合物之一,在制药、化妆品、农业和食品行业等有着广泛的应用。比较常见的单萜类化合物有香叶醇、芳樟醇、香茅酸、樟脑、薄荷醇等,对人类的日常生活有着举足轻重的作用。但由于常见的天然环状单萜的骨架是有限的,限制了单萜类化合物在药物研发以及其他方面的应用。
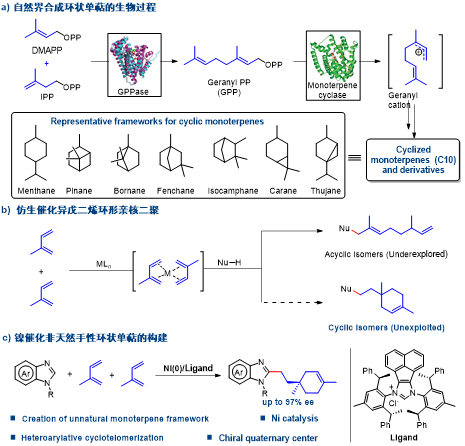
作为廉价易得的大宗化学品,异戊二烯的高附加值转化一直是学术界和工业界关注的焦点,其在理论上是高原子经济性构建单萜的理想前体。但是,由于异戊二烯共轭双键具有的相似的电子效应和位阻效应,使得反应的区域选择性和立体选择性难以有效的控制。另外之前的工作表明,异戊二烯的直接氢官能化比亲核二聚反应更容易实现,使得反应的化学选择性调控更加困难。目前关于异戊二烯合成单萜的研究,仅仅局限于非手性非环状单萜的报道。另一方面杂环化合物,如嘌呤和咪唑,在药物和天然产物中发挥着重要作用。因此,人们广泛致力于这些化合物的功能化研究。其中,过渡金属催化的C-H官能化过程具有高效的原子和步骤经济性,是当今化学催化领域的研究前沿。那么,将过渡金属催化的C-H键活化与异戊二烯的多样性转化结合起来,将会是一个非常有趣且有实际应用价值的研究领域。
本工作中,该团队受单萜化合物生物合成的启发,发展了一种新颖的镍催化异戊二烯的不对称杂芳基化环化催化体系。由廉价金属镍和手性大位阻卡宾配体组成的催化体系,实现了一系列非天然单萜衍生物高产率、高区域选择性以及高立体选择性合成。机理研究表明,该反应首先在镍催化下通过异戊二烯自身二聚,形成手性环状单萜中间体。随后,通过镍催化的sp2 C-H键烷基化,实现一系列含有季碳手性中心的非天然环状单萜衍生物的高效构建。此外,当将异戊二烯替换为更长链的单萜、倍半萜以及二萜类似物时,反应也能很好地兼容,进一步证明了该反应策略的普适性。该策略不仅为异戊二烯的高附加值转化提供了新思路,同时也对非天然手性环状单萜的合成具有借鉴意义。
陈庆安团队一直致力于发展不同催化体系,以实现大宗化学品的催化转化。在前期工作中,团队分别发展了“金属调控”的策略实现了异戊二烯氢芳基化,“配体调控”的策略实现了氢硅基化、“添加物调控”的策略实现了氢氨化以及氢烷基化(Angew. Chem. Int. Ed.,2019;Chem. Sci.,2019;Chin. J. Catal.,2020;Angew. Chem. Int. Ed.,2020;Angew. Chem. Int. Ed.,2021;Angew. Chem. Int. Ed.,2022;ACS Catal.,2022;Trends in Chem.,2022)等多样性转化,此外,还对异戊烯醇及其类似物进行了相关研究,通过“氧化还原调控”的策略实现了酮类化合物与异戊烯醇的氧化偶联以及噻吩、二氢噻吩及其衍生物的快速程序化合成(Angew. Chem. Int. Ed.,2021;ACS Catal.,2021;Chin. J. Catal.,2021)。
相关研究成果以“Nickel-Catalysed Asymmetric Heteroarylative Cyclotelomerization of Isoprene” 为题,于近日发表在《自然-催化》(Nature Catalysis)上。该工作的第一作者是我所211组博士研究生张功。上述研究工作得到了国家自然科学基金等项目的资助。(文/图 张功)






