近日,我所生物分子结构表征新方法研究组(1822组)王方军研究员、刘哲益副研究员团队与西南交通大学封顺教授团队合作,利用我所自主搭建的高能紫外激光解离—串联质谱仪器,揭示了质子化氨基酸侧链的正电荷在电喷雾离子化过程中影响蛋白质结构的分子机制,为质谱精确表征蛋白质高级结构提供了参考。
非变性质谱(nMS)是研究蛋白质及其复合物组成和高级结构的前沿质谱技术。在nMS分析中采用生物兼容溶液和非变性电喷雾离子化将蛋白质从液相转移至气相并保持高级结构和相互作用。然而带正电荷的质子化氨基酸侧链在失去水分子的溶剂化稳定作用后,会与空间接近的蛋白骨架羰基形成氢键,通过分子内溶剂化稳定侧链正电荷。虽然有报道通过离子迁移—质谱检测到了分子内溶剂化引起的蛋白质碰撞截面积变化,但是对其发生的具体位点和引起结构变化的区域仍然缺乏有效分析手段进行精确表征。
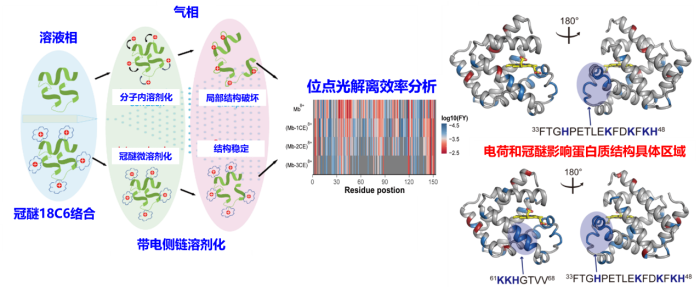
在本工作中,研究团队利用我所自主搭建的高能紫外激光解离—串联质谱仪器和蛋白质光解离质谱数据处理软件系统,通过蛋白质紫外光解离碎片离子的价态分布和位点解离碎片产率分析,探测到肌红蛋白带电残基侧链分子内溶剂化的具体位点,以及对蛋白质结构影响的区域位置。团队系统表征了不同价态(质子化数目)下的蛋白质结构差异,发现高电荷价态下蛋白质气相结构易受分子内溶剂化效应的影响而偏离溶液态结构,低电荷蛋白质离子的气相结构更加接近溶液状态。研究团队进一步证明,冠醚18C6与蛋白质带电侧链的络合主要发生在溶液中,随后在电喷雾离子化过程中起到稳定蛋白质结构的作用。紫外激光解离质谱分析揭示冠醚主要结合在蛋白质离子的高电荷密度区域,通过阻断带电侧链的分子内溶剂化使蛋白质气相结构更加接近溶液状态。相关研究结果展示了高能紫外激光解离质谱在同时获取蛋白质序列和动态结构信息中的显著优势,为nMS表征中蛋白质溶液结构的保持和高效表征提供了重要的理论和技术参考。
近年来,我所王方军和肖春雷研究员通过交叉学科联合创新攻关,在大连相干光源搭建了高能紫外激光解离—串联质谱实验线站,兼容50-150nm极紫外自由电子激光和193nm准分子激光解离模式,已在多肽(Anal. Chim. Acta,2021)、蛋白质(Cell Chem. Biol.,2022)、金属团簇(J. Phys. Chem. Lett.,2020;Sci. China Chem,2022)等大分子体系的解离和结构表征中取得了系列研究成果。
相关研究成果以“Ultraviolet Photodissociation Reveals the Molecular Mechanism of Crown Ether Microsolvation Effect on the Gas-Phase Native-like Protein Structure”为题,于近日发表在《美国化学会志》(Journal of the American Chemical Society)上。该工作的共同第一作者是我所1822组联合培养硕士研究生周伶强和刘哲益。(文/图 刘哲益、周伶强)






